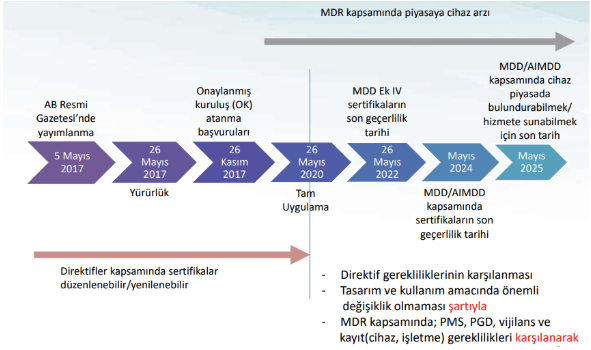
Bilindiği gibi Avrupa Tıbbi Cihaz Regülasyonu (Medical Device Regulation/MDR) 5 Nisan 2017 tarihinde (2017/745 / EC) Avrupa Parlamentosu tarafından kabul edilmiştir. Avrupa Tıbbi Cihaz Regülasyonu 26 Mayıs 2020'de yürürlüğe girecektir. MDR geçiş hükümleri çerçevesinde, Ocak 2019 ile Mayıs 2020 arasındaki dönem özellikle tıbbi cihaz üreticileri için ciddi bir önem arz etmektedir.
Tıbbi Cihaz Regülasyonu, AIMDD/MDD içerisine dahil olmayan bazı ürünler için genişletilmiştir. Tıbbi cihazlara benzer özelliklere sahip olan ancak tıbbi bir amaç taşımayan, implante edilebilir ya da diğer invaziv ürünlerde (ör: düzeltici özellikte olmayan kontakt lensler, estetik amaçlı yapılan implantlar, dermal dolgular, liposuction ekipmanları ) regülasyon kapsamına dahil edilmiştir.
2010/227/EU Komisyon Kararı uyarınca; Avrupa Veri Bankası’na (EUDAMED) piyasaya arz edilen tıbbi cihazların Tıbbi Cihaz Regülasyonu gereğince
26 Mayıs 2020 tarihinden sonra Onaylanmış kuruluşlar, gözetim denetimlerinde Avrupa Tıbbi Cihaz Regülasyonu’ nun piyasaya arz sonrası gözetim, piyasa gözetimi şartlarına uygun olarak denetimlerini gerçekleştirecektir.
Medikal Cihaz Direktifleri 60 sayfa, 23 Madde ve toplam 12 ekten oluşurken; Medikal Cihaz Regülasyonu 175 sayfa,123 Madde ve 16 ekten oluşmaktadır. Bu anlamda gereklilikler ve zorunluluklar oldukça artmaktadır.